![]() KÖVESSE
KÖVESSE
A barcelonai Genomikus Szabályozási Központ (CRG) tudományos csoportja által kifejlesztett új innovatív technika számos „távirányító” létezését fedezte fel, amelyek szabályozzák a fehérjék működését, és célpontként használhatók hatékonyabb gyógyszerek előállításához. és hatékony különféle patológiákban, például demencia, rák és fertőző fertőzések esetén.
Ezeket a „távirányítókat” tudományosan alloszterikus helyekként ismerik. Ezek olyan távirányítók, amelyek távol vannak a fehérje hatásának helyétől, de rendelkeznek szabályozó vagy moduláló képességgel" - magyarázta az ABC-nek Júlia Domingo, a tanulmány első társszerzője, amely szerdán jelent meg a "Natura" magazinban. . És hozzátesz egy hasonlatot: „Olyan, mintha azzal a távirányítóval be- és kikapcsolhatná az izzót, vagy szabályozná a fény intenzitását.”
Ebben az esetben olyan fehérjék aktivitásának blokkolása vagy szabályozása, amelyek megtartják megváltozott funkciójukat zártságban. Például a rák esetében a mutációt elsajátított fehérjék működése megváltozik, abnormális módon teszik ezt, és a sejt furcsa módon nő. Sok esetben nincsenek olyan gyógyszerek, amelyek módosítanák vagy blokkolhatnák ezt a kóros aktivitást, vagy ha vannak, nem specifikusak, és más, normálisan működő fehérjékből is felszabadulnak.
Hagyományosan a drogvadászok olyan kezeléseket terveztek, amelyek egy fehérje aktív helyét célozzák meg, amelynek kis régiója kémiai reakciókat vált ki, ahol a célpontok megkötődnek. Ezeknek az ortoszterikus gyógyszereknek nevezett gyógyszerek hátránya, hogy sok fehérje aktív helye nagyon hasonló, és a gyógyszerek egyszerre sok különböző fehérjét kötöttek és gátolnak, még azokat is, amelyek normálisan működnek, és nem érdemes megérinteni őket. mellékhatásokat okoznak.
„Ott belépett az allosztéria fogalmába és a benne rejlő lehetőségekbe a gyógyszerek tervezésében. Az alloszterikus helyek érdekessége, hogy szuperspecifikusak minden egyes fehérjére. Ha ezek az alloszterikus helyek megtalálják a fehérje felszínének azt a részét, ahol a gyógyszer elérheti, az rendkívül specifikus lesz az adott fehérjére. Törekedhetünk hatékonyabb gyógyszerekre” – mondja a kutató.
„Nemcsak azt tapasztaljuk, hogy ezek a terápiás helyek bőségesek, de bizonyíték van arra is, hogy sokféle módon manipulálhatók. Ahelyett, hogy csak be- és kikapcsolnánk őket, termosztátszerűen modulálhatjuk a tevékenységüket. Mérnöki szempontból olyan, mintha aranyat vertünk volna, mert ez nagy teret ad nekünk olyan „okos gyógyszerek” tervezésére, amelyek rosszat tesznek, és kihagyják a jót” – magyarázza André Faure, a CRG posztdoktori kutatója. és a cikk első társszerzője.
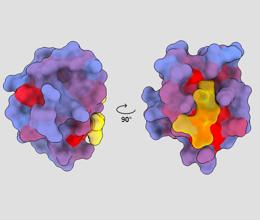 Háromdimenziós kép, amely a PSD95-PDZ3 humán fehérjét mutatja különböző nézőpontokból. Az aktív helyhez kötődő molekula sárga színnel látható. A kéktől a pirosig tartó gradiens lehetséges alloszterikus helyeket jelez – André Faure/ChimeraX
Háromdimenziós kép, amely a PSD95-PDZ3 humán fehérjét mutatja különböző nézőpontokból. Az aktív helyhez kötődő molekula sárga színnel látható. A kéktől a pirosig tartó gradiens lehetséges alloszterikus helyeket jelez – André Faure/ChimeraX
Ehhez a felfedezéshez a csapat olyan módszert alkalmazott, amely lehetővé teszi számukra, hogy fehérjét és szisztémás formát vegyenek fel, és globális találkozást végezzenek minden hellyel. Ennek érdekében két nagyon bőséges fehérjét választottak ki emberi proteomunkban. „A fehérjefelület 50%-a alloszterikus potenciállal rendelkezik. Módszerünk lehetővé teszi, hogy létrehozzuk az allosztérikus helyek atlaszát, ami sokkal hatékonyabbá tenné a hatékony gyógyszerek felkutatásának folyamatát” – mondja Domingo Júlia.
A tanulmány szerzői a kettős mélységű PCA (ddPCA) nevű technikát fejlesztették ki, amelyet "durva erő kísérletként" írnak le. „Szándékosan bontjuk szét a dolgokat több ezer különböző módon, hogy teljes képet alkothassunk arról, hogyan működik valami” – magyarázza Ben Lehner, az ICREA kutatóprofesszora, a CRG Systems Biology program koordinátora és a tanulmány szerzője. „Olyan, mintha azt gyanítaná, hogy egy gyújtógyertya nem működik, de ahelyett, hogy ezt ellenőrizné, a szerelő szétszedi az egész autót, és egyenként ellenőrzi az összes alkatrészt. Tízezer dolgot egyszerre elemezve azonosítjuk az összes igazán fontos darabot.”
Ezután mesterséges intelligencia algoritmusokat használunk a laboratóriumi eredmények értelmezésére.
A módszer egyik nagy előnye amellett, hogy leegyszerűsíti az allosztérikus helyek megtalálásához szükséges folyamatot, hogy megfizethető és elérhető technika a világ bármely kutatólaboratóriumában. „Csak az alapvető molekuláris biológiai reagensekhez, egy DNS-szekvenálóhoz és egy számítógéphez kell hozzáférni. Ezzel a három komponenssel bármely laboratórium 2-3 hónap alatt, kis költségvetéssel elvégezheti ezt a kísérletet a kívánt fehérjével” – mondja Domingo Júlia. A kutatók azt remélik, hogy tudósaink a technikával gyorsan és átfogóan feltérképezhetik az emberi fehérjék allosztérikus helyeit egyenként. „Ha elegendő adatunk van, talán egy nap még egy lépéssel tovább léphetünk, és mindent megjósolhatunk a fehérjék sorrendjétől a funkciójukig. Használja ezeket az adatokat arra, hogy jobb terápiákként irányítsák őket, hogy megjósolhassák, ha egy fehérje bizonyos változása betegséggé fajul-e” – összegezte a kutató.