![]() ПРАТИТИ
ПРАТИТИ
Нова иновативна техника коју је развио научни тим у Центру за геномску регулацију (ЦРГ) у Барселони открила је постојање мноштва 'даљинских управљача' који контролишу функцију протеина и који се могу користити као мете за постизање ефикаснијих лекова. и ефикасан у разним патологијама као што су деменција, рак и заразне инфекције.
Ове 'даљинске контроле' су научно познате као алостерична места. То су даљински управљачи који су удаљени од места деловања протеина, али имају капацитет да га регулишу или модулирају“, Јулиа Доминго, прва коауторка студије, која је објављена ове среде у часопису „Натуре“, објаснио за АБЦ. И додаје поређење: „Као да са тим даљинским управљачем можете палити и гасити сијалицу или регулисати интензитет светлости.
У овом случају када намерава да блокира или регулише активност протеина који одржавају своју измењену функцију у затвореном простору. На пример, у случају рака, протеини који су добили мутацију имају промењену функционалност, они то раде ненормално и ћелија расте необично. У многим случајевима, не постоје лекови који могу модулирати или блокирати ову абнормалну активност или, ако постоје, нису специфични и такође се ослобађају из других протеина који нормално функционишу.
Традиционално, ловци на дроге су осмислили третмане који циљају на активно место протеина, чији мали регион производи хемијске реакције где се мете везују. Недостатак ових лекова, познатих као ортостерични лекови, је то што су активна места многих протеина веома слична и лекови су везали и инхибирали много различитих протеина у исто време, чак и оне који нормално функционишу и нису интересантни за додир, који може изазвати нежељене ефекте.
„Тамо је ушао у концепт алостерије и потенцијала који има за дизајнирање лекова. Занимљива ствар код алостеричних места је да су супер специфичне за сваки протеин. Ако ова алостерична места пронађу део површине протеина где лек може да слети, он ће бити изузетно специфичан за тај протеин. Моћи ћемо да тежимо ефикаснијим лековима“, истиче истраживач.
„Не само да откривамо да су ова терапеутска места у изобиљу, већ постоје докази да се њима може манипулисати на много различитих начина. Уместо да их само укључујемо и искључујемо, можемо да модулирамо њихову активност као термостат. Са инжењерске тачке гледишта, као да смо погодили злато, јер нам то даје много простора да дизајнирамо 'паметне лекове' који иду у лоше, а прескачу добро", објашњава Андре Фауре, постдокторски истраживач на ЦРГ-у. и први коаутор чланка.
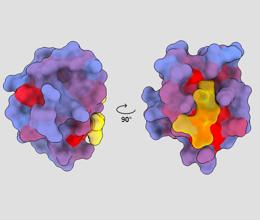 тродимензионална слика која приказује људски протеин ПСД95-ПДЗ3 са различитих тачака гледишта. Жутом бојом је приказан молекул који се везује за активно место. Плаво-црвени градијент боје указује на могућа алостерична места – Андре Фауре/ЦхимераКс
тродимензионална слика која приказује људски протеин ПСД95-ПДЗ3 са различитих тачака гледишта. Жутом бојом је приказан молекул који се везује за активно место. Плаво-црвени градијент боје указује на могућа алостерична места – Андре Фауре/ЦхимераКс
За ово откриће, тим је користио методу која им омогућава да узму протеин и системски облик и глобални сусрет са свим локацијама. Да би то урадили, изабрали су два веома богата протеина у нашем људском протеому. „50% површине протеина има алостерични потенцијал. Наш метод омогућава да се направи атлас алостеричних места, чиме би процес тражења ефикасних лекова био много ефикаснији“, уверава Јулија Доминго.
Аутори студије развили су технику названу ПЦА двоструке дубине (ддПЦА), коју описују као „експеримент грубе силе“. „Намјерно разбијамо ствари на хиљаде различитих начина како бисмо створили потпуну слику о томе како нешто функционише“, објашњава ИЦРЕА истраживачки професор Бен Лехнер, координатор програма системске биологије на ЦРГ-у и аутор студије. „То је као да сумњате да је свећица лоша, али уместо да то само провери, механичар ће раставити цео ауто и проверити све делове један по један. Анализирајући десет хиљада ствари одједном, идентификујемо све делове који су заиста важни.”
Затим користимо алгоритме вештачке интелигенције за тумачење лабораторијских резултата.
Једна од великих предности методе, поред поједностављивања процеса неопходног за проналажење алостеричних места, јесте то што је приступачна и приступачна техника за сваку истраживачку лабораторију у свету. „То само захтева приступ основним реагенсима молекуларне биологије, приступ ДНК секвенцеру и рачунару. Са ове три компоненте, свака лабораторија за 2-3 месеца, са малим буџетом, може да изведе овај експеримент на протеину од интереса који жели“, уверава Јулија Доминго. Истраживачи се надају да ће наши научници користити технику да брзо и свеобухватно мапирају алостерична места људских протеина један по један. „Ако имамо довољно података, можда једног дана можемо отићи корак даље и предвидети од секвенце протеина до функције. Користите ове податке да их водите као боље терапије за предвиђање да ли ће се одређена промена у протеину дегенерисати у болест“, закључио је истраживач.
