![]() NASLEDNJE
NASLEDNJE
Nova inovativna tehnika, ki jo je razvila znanstvena skupina v Centru za genomsko regulacijo (CRG) v Barceloni, je odkrila obstoj množice "daljinskih upravljalnikov", ki nadzorujejo delovanje beljakovin in jih je mogoče uporabiti kot cilje za doseganje učinkovitejših zdravil. in učinkovit pri različnih patologijah, kot so demenca, rak in nalezljive okužbe.
Ti "daljinski upravljalniki" so znanstveno znani kot alosterična mesta. To so daljinski upravljalniki, ki so oddaljeni od mesta delovanja proteina, vendar imajo sposobnost, da ga uravnavajo ali modulirajo," Júlia Domingo, prva soavtorica študije, ki je to sredo objavljena v reviji "Nature", je pojasnil ABC. In dodaja primerjavo: "Kot da bi s tem daljinskim upravljalnikom lahko prižigali in ugašali žarnico ali uravnavali jakost svetlobe."
V tem primeru, ko namerava blokirati ali uravnavati aktivnost beljakovin, ki ohranjajo svojo spremenjeno funkcijo v zaprtju. Na primer, v primeru raka se beljakovinam, ki so pridobile mutacijo, spremeni njihova funkcionalnost, to počnejo nenormalno in celica nenavadno raste. V mnogih primerih ni zdravil, ki bi lahko modulirali ali blokirali to nenormalno aktivnost ali, če obstajajo, niso specifična in se sproščajo tudi iz drugih beljakovin, ki delujejo normalno.
Tradicionalno so lovci na droge zasnovali zdravljenje, ki cilja na aktivno mesto proteina, katerega majhna regija proizvaja kemične reakcije, kjer se tarče vežejo. Pomanjkljivost teh zdravil, znanih kot ortosterična zdravila, je, da so aktivna mesta številnih beljakovin zelo podobna in da so zdravila hkrati vezala in zavirala veliko različnih beljakovin, tudi tistih, ki normalno delujejo in jih ni zanimivo dotikati, lahko povzroči neželene učinke.
»Tam je vstopil v koncept alosterije in potenciala, ki ga ima pri oblikovanju zdravil. Zanimivost pri alosteričnih mestih je, da so zelo specifična za vsako beljakovino. Če ta alosterična mesta najdejo del površine beljakovin, kjer lahko zdravilo pristane, bo za to beljakovino izjemno specifično. Lahko si bomo prizadevali za učinkovitejša zdravila,« poudarja raziskovalka.
"Ne samo, da ugotovimo, da je teh terapevtskih mest veliko, ampak obstajajo dokazi, da je z njimi mogoče manipulirati na različne načine. Namesto da bi jih samo vklopili in izklopili, lahko moduliramo njihovo aktivnost kot termostat. Z inženirskega vidika je tako, kot da smo dosegli zlato, saj nam daje veliko prostora za oblikovanje 'pametnih zdravil', ki gredo v slabo in preskočijo dobro," pojasnjuje André Faure, podoktorski raziskovalec na CRG. in prvi soavtor članka.
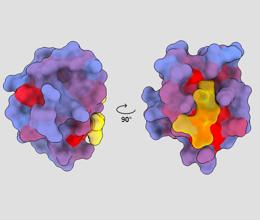 tridimenzionalna slika, ki prikazuje človeški protein PSD95-PDZ3 z različnih zornih kotov. Molekula, ki se veže na aktivno mesto, je prikazana rumeno. Modro do rdeče barvni gradient označuje možna alosterična mesta – André Faure/ChimeraX
tridimenzionalna slika, ki prikazuje človeški protein PSD95-PDZ3 z različnih zornih kotov. Molekula, ki se veže na aktivno mesto, je prikazana rumeno. Modro do rdeče barvni gradient označuje možna alosterična mesta – André Faure/ChimeraX
Za to odkritje je ekipa uporabila metodo, ki jim omogoča, da prevzamejo beljakovinsko in sistemsko obliko ter globalno srečanje z vsemi mesti. Za to so izbrali dva zelo bogata proteina v našem človeškem proteomu. »50 % površine beljakovin ima alosterični potencial. Naša metoda omogoča izdelavo atlasa alosteričnih mest, s čimer bi bil proces iskanja učinkovitih zdravil veliko učinkovitejši,« zagotavlja Júlia Domingo.
Avtorji študije so razvili tehniko, imenovano dvojna globina PCA (ddPCA), ki jo opisujejo kot "eksperiment s surovo silo". "Zadeve namenoma razbijemo na tisoče različnih načinov, da ustvarimo popolno sliko o tem, kako nekaj deluje," pojasnjuje raziskovalni profesor ICREA Ben Lehner, koordinator programa sistemske biologije pri CRG in avtor študije. »To je tako, kot če sumite, da je vžigalna svečka slaba, a namesto da bi to samo preveril, bo mehanik razstavil cel avto in preveril vse dele enega za drugim. Z analizo deset tisoč stvari naenkrat identificiramo vse dele, ki so resnično pomembni.
Nato uporabljamo algoritme umetne inteligence za interpretacijo laboratorijskih rezultatov.
Ena od velikih prednosti metode, poleg poenostavitve postopka, potrebnega za iskanje alosteričnih mest, je, da je cenovno ugodna in dostopna tehnika za kateri koli raziskovalni laboratorij na svetu. »Potrebuje le dostop do osnovnih reagentov molekularne biologije, dostop do sekvencerja DNK in računalnika. S temi tremi komponentami lahko vsak laboratorij v 2-3 mesecih z majhnim proračunom izvede ta poskus na beljakovinah, ki jih zanima,« zagotavlja Júlia Domingo. Raziskovalci upajo, da bodo naši znanstveniki uporabili tehniko za hitro in celovito preslikavo alosteričnih mest človeških beljakovin enega za drugim. »Če imamo dovolj podatkov, bomo morda nekega dne lahko šli še korak dlje in napovedali od zaporedja beljakovin do delovanja. Uporabite te podatke, da jih vodite kot boljše terapije za napovedovanje, ali se bo določena sprememba v proteinu sprevrgla v bolezen,« je zaključil raziskovalec.