![]() Հաջորդ
Հաջորդ
Բարսելոնայի Գենոմատիկ կարգավորման կենտրոնի (CRG) գիտական խմբի կողմից մշակված նոր նորարարական տեխնիկան հայտնաբերել է բազմաթիվ «հեռակառավարման սարքերի» առկայությունը, որոնք վերահսկում են սպիտակուցների գործառույթը և կարող են օգտագործվել որպես թիրախ՝ ավելի արդյունավետ դեղամիջոցներ ձեռք բերելու համար։ և արդյունավետ տարբեր պաթոլոգիաների դեպքում, ինչպիսիք են թուլամտությունը, քաղցկեղը և վարակիչ վարակները:
Այս «հեռակառավարման սարքերը» գիտականորեն հայտնի են որպես ալոստերիկ տեղամասեր: Սրանք հեռակառավարման վահանակներ են, որոնք հեռու են սպիտակուցի գործողության վայրից, բայց ունեն այն կարգավորելու կամ մոդուլացնելու կարողություն»,- այս չորեքշաբթի «Nature» ամսագրում հրապարակված հետազոտության առաջին համահեղինակ Ջուլիա Դոմինգոն։ բացատրել է ABC-ին։ Եվ նա ավելացնում է նմանություն. «Կարծես այդ հեռակառավարման վահանակով կարելի է միացնել-անջատել լամպը կամ կարգավորել լույսի ուժգնությունը»։
Այս դեպքում, երբ այն մտադիր է արգելափակել կամ կարգավորել սպիտակուցների գործունեությունը, որոնք պահպանում են իրենց փոփոխված գործառույթը կալանքի տակ: Օրինակ՝ քաղցկեղի դեպքում մուտացիա ձեռք բերած սպիտակուցները փոխվել են իրենց ֆունկցիոնալությունը, նրանք դա անում են աննորմալ կերպով, և բջիջը աճում է անսովոր ձևով։ Շատ դեպքերում չկան դեղամիջոցներ, որոնք կարող են մոդուլավորել կամ արգելափակել այս աննորմալ գործունեությունը, կամ, եթե կան, դրանք հատուկ չեն և նույնպես ազատվում են նորմալ գործող այլ սպիտակուցներից:
Ավանդաբար, թմրամիջոցների որսորդները մշակել են բուժման մեթոդներ, որոնք ուղղված են սպիտակուցի ակտիվ կայքին, որի փոքր հատվածը քիմիական ռեակցիաներ է առաջացնում, որտեղ թիրախները կապվում են: Այս դեղերի թերությունը, որոնք հայտնի են որպես օրթոստերիկ դեղամիջոցներ, այն է, որ շատ սպիտակուցների ակտիվ տեղամասերը շատ նման են, և դեղամիջոցները միաժամանակ միացրել և արգելակել են բազմաթիվ տարբեր սպիտակուցներ, նույնիսկ նրանք, որոնք նորմալ են գործում և հետաքրքիր չեն դիպչել, որոնք: կարող է առաջացնել կողմնակի բարդություններ:
«Այնտեղ նա մտավ ալոստերիայի հայեցակարգը և այն ներուժը, որն այն ունի դեղամիջոցներ նախագծելու համար: Հետաքրքիրն ալոստերիկ տեղամասերի վերաբերյալ այն է, որ դրանք չափազանց հատուկ են յուրաքանչյուր սպիտակուցի համար: Եթե այս ալոստերիկ տեղամասերը գտնեն սպիտակուցի մակերեսի մի մասը, որտեղ դեղը կարող է վայրէջք կատարել, այն չափազանց հատուկ կլինի այդ սպիտակուցի համար: Մենք կկարողանանք ձգտել ավելի արդյունավետ դեղամիջոցների»,- նշում է հետազոտողը։
«Ոչ միայն մենք գտնում ենք, որ այս բուժական վայրերն առատ են, այլև ապացույցներ կան, որ դրանք կարելի է տարբեր ձևերով շահարկել: Պարզապես դրանք միացնելու և անջատելու փոխարեն՝ մենք կարող ենք թերմոստատի նման մոդուլացնել դրանց ակտիվությունը: Ինժեներական տեսանկյունից մենք կարծես ոսկի ենք խփել, քանի որ այն մեզ շատ տեղ է տալիս «խելացի դեղամիջոցներ» նախագծելու համար, որոնք գնում են դեպի վատը և բաց թողնում լավը», - բացատրում է Անդրե Ֆորը՝ CRG-ի հետդոկտորական գիտաշխատող։ և առաջին՝ հոդվածի համահեղինակ։
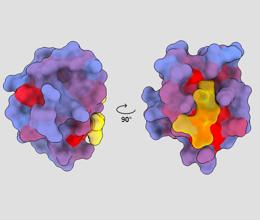 եռաչափ պատկեր, որը ցույց է տալիս մարդկային PSD95-PDZ3 սպիտակուցը տարբեր տեսանկյուններից: Դեղին գույնով ցուցադրվում է մոլեկուլ, որը կապված է ակտիվ վայրի հետ: Կապույտից կարմիր գույնի գրադիենտը ցույց է տալիս հնարավոր ալոստերիկ տեղամասերը՝ Անդրե Ֆոր/ChimeraX
եռաչափ պատկեր, որը ցույց է տալիս մարդկային PSD95-PDZ3 սպիտակուցը տարբեր տեսանկյուններից: Դեղին գույնով ցուցադրվում է մոլեկուլ, որը կապված է ակտիվ վայրի հետ: Կապույտից կարմիր գույնի գրադիենտը ցույց է տալիս հնարավոր ալոստերիկ տեղամասերը՝ Անդրե Ֆոր/ChimeraX
Այս հայտնագործության համար թիմը օգտագործել է մեթոդ, որը թույլ է տալիս նրանց ընդունել սպիտակուց և համակարգային ձև և գլոբալ հանդիպում բոլոր կայքերի հետ: Դա անելու համար նրանք ընտրել են երկու շատ առատ սպիտակուցներ մեր մարդկային պրոտեոմում: «Սպիտակուցի մակերեսի 50%-ն ունի ալոստերիկ պոտենցիալ: Մեր մեթոդը հնարավորություն է տալիս ստեղծել ալոստերիկ վայրերի ատլաս, որը շատ ավելի արդյունավետ կդարձներ արդյունավետ դեղերի որոնման գործընթացը»,- վստահեցնում է Ջուլիա Դոմինգոն։
Հետազոտության հեղինակները մշակել են մի տեխնիկա, որը կոչվում է կրկնակի խորության PCA (ddPCA), որը նրանք նկարագրում են որպես «բիրտ ուժի փորձ»: «Մենք միտումնավոր կոտրում ենք իրերը հազարավոր տարբեր ձևերով՝ ամբողջական պատկերացում կազմելու համար, թե ինչպես է ինչ-որ բան աշխատում», - բացատրում է ICREA հետազոտող պրոֆեսոր Բեն Լեները՝ CRG-ի Systems Biology ծրագրի համակարգող և հետազոտության հեղինակ: «Կարծես եթե կասկածում ես, որ մոմը վատն է, բայց դա պարզապես ստուգելու փոխարեն, մեխանիկը կքանդի ամբողջ մեքենան և հերթով կստուգի բոլոր մասերը: Միանգամից տասը հազար բան վերլուծելով՝ մենք բացահայտում ենք բոլոր այն կտորները, որոնք իսկապես կարևոր են»։
Հաջորդը, մենք օգտագործում ենք արհեստական ինտելեկտի ալգորիթմներ՝ լաբորատոր արդյունքները մեկնաբանելու համար:
Մեթոդի մեծ առավելություններից մեկը, բացի ալոստերիկ տեղամասեր գտնելու համար անհրաժեշտ գործընթացի պարզեցումից, այն է, որ այն մատչելի և հասանելի տեխնիկա է աշխարհի ցանկացած հետազոտական լաբորատորիայի համար: «Դա պարզապես պահանջում է մուտք դեպի հիմնական մոլեկուլային կենսաբանության ռեագենտներ, մուտք դեպի ԴՆԹ հաջորդականացուցիչ և համակարգիչ: Այս երեք բաղադրիչներով ցանկացած լաբորատորիա 2-3 ամսում, փոքր բյուջեով, կարող է այս փորձն իրականացնել իրենց ուզած հետաքրքրության սպիտակուցի վրա»,- վստահեցնում է Ջուլիա Դոմինգոն։ Հետազոտողների հույսն այն է, որ մեր գիտնականները կօգտագործեն տեխնիկան արագ և համապարփակ կերպով մարդկային սպիտակուցների ալոստերիկ վայրերը մեկ առ մեկ քարտեզագրելու համար: «Եթե մենք բավականաչափ տվյալներ ունենանք, գուցե մի օր մենք կարողանանք մեկ քայլ առաջ գնալ և կանխատեսել սպիտակուցների հաջորդականությունից մինչև գործառույթ: Օգտագործեք այս տվյալները՝ դրանք առաջնորդելու համար որպես ավելի լավ թերապիա՝ կանխատեսելու, թե արդյոք սպիտակուցի որոշակի փոփոխությունը կվերածվի հիվանդության», - եզրափակել է հետազոտողը:
